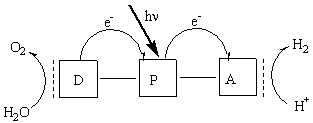
La photosynthèse artificielle
Le but de la photosynthèse artificielle est de reproduire l’habilité des plantes vertes d’utiliser la lumière solaire pour synthétiser des produits chimiques de haute énergie. Pendant plusieurs années, différents systèmes ont été réalisés, avec lesquels on a essayé de reproduire le processus de la photosynthèse naturelle. La représentation schématique d’un potentiel dispositif photosynthétique artificiel est présentée dans la Figure 1 et consiste de differents accepteurs (A) et donneurs (D) d’électrons, qui peuvent réaliser les fonctionnes de la photosynthèse naturelle.
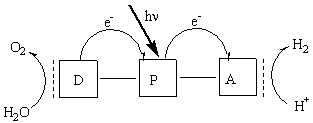
Figure 1 La représentation schématique d’un dispositif photosynthétique artificiel
(P = photosensibilisateur; A = accepteur d’électron; D = donneur d’électron )
L’élément clé de la photosynthèse artificielle sera la formation d’un état avec des charges séparées avec une durée de vie assez longue, qui pourrait réagir avec l’eau pour former hydrogène et d’autres composés de haute énergie (oxygène).
Il y a une gamme large de matériaux qui peuvent produire des systèmes de type charges séparées, en se comportant dans la même manière que les chlorophylles et caroténoïdes alors qu’elles absorbent de la lumière dans la photosynthèse naturelle. Parmi ces matériaux, une classe importante est constituée par les complexes métalliques, dans lesquels nous sommes intéressés. Par exemple, les complexes des métaux d6 avec des ligands polypyridiles montrent une modification de l’état excité du complexe en changeant l'ion métallique. À partir de la Figure 2 1 on peut observer un plus large dédoublage pour les orbitales métalliques d (t2g et eg) avec l’augmentation de la force du champ de ligand.
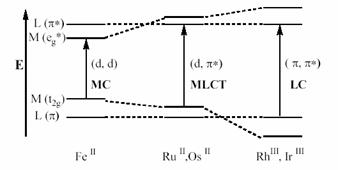
Figure 2. Diagramme d’énergie pour les complexes avec la configuration d6
À partir du diagramme d’énergies présenté ci-dessus, quelques conclusions peuvent être faites. Pour la première série, les complexes de Fe(II) présentent des transitions dd centrées sur métal pour HOMO (t2g) et LUMO (eg). Pour la deuxième ou troisième série, Ru(II) ou Os(II), les orbitales LUMO sont les orbitales p* basées sur ligand, à cause que le champ de ligand des métaux lourds est plus fort. Ça veut dire que, alors que les complexes de Ru où Os avec des ligands polypyridiles sont photoexcités, l’électron passe du métal au ligand, en produisant un état excité de type charge séparée. Par excitation d’un complexe de ruthénium avec des ligands polypyridiles, Ru(II) est oxydé au Ru(III), tandis que le ligand est réduit à l’anion radical.2
Un tel système avec des charges séparées ressemble à la photosynthèse naturelle.
[1] Kalyanasundaram, K. Photochemistry of polypyridine and porphyrin complexes, Academic Press: London, 1992.